Selpercatinib beim RET+ NSCLC
Selpercatinib ist zugelassen zur Therapie des fortgeschrittenen RET+ NSCLC bei Patientinnen und Patienten (Pat.), die zuvor nicht mit einem RET-Inhibitor behandelt wurden. Der G-BA hat das IQWiG mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
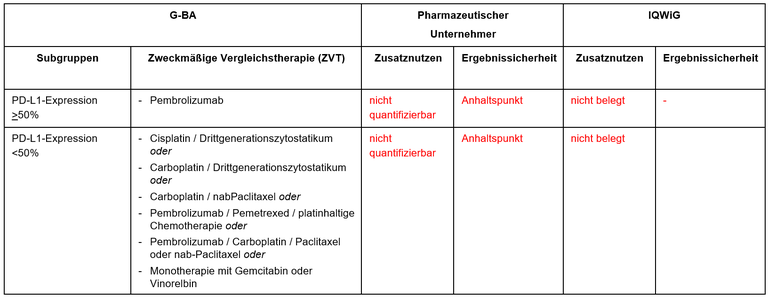
Unsere Anmerkungen sind:
- Die Festlegung der ZVT entspricht nicht mehr den aktuellen Leitlinien und dem Standard der Versorgung. Standard ist die kombinierte Immunchemotherapie, sie wird auch bei einer hohen Expression von PD-L1 empfohlen. Gleichzeitig reicht das Spektrum der empfohlenen Immunchemotherapie über Pembrolizumab hinaus. Eine Chemotherapie ohne Immuncheckpoint-Inhibitor ist nicht akzeptabel außer bei Pat. mit Kontraindikationen.
- Basis der frühen Nutzenbewertung ist LIBRETTO-001, eine offene, internationale, multizentrische Phase-1/2-Basket-Studie. Ausgewertet wurden 69 Pat. mit lokal fortgeschrittenem oder metastasiertem, nicht systemisch vorbehandeltem RET+ NSCLC.
- Selpercatinib führte bei 84% der Pat. zu einer Remission, dominierend zu einer partiellen Remission. Die mediane progressionsfreie Überlebensrate lag bei etwa 22 Monaten, die Gesamtüberlebensrate nach 2 Jahren bei 70%.
- Im intraindividuellen Vergleich zeigten sich Verbesserung des Patient-Reported-Outcome und der Lebensqualität.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Selpercatinib den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Die hier separat ausgewerteten Daten bei nicht systemisch vorbehandelten Pat. mit RET+ NSCLC bestätigen die hohe Wirksamkeit von Selpercatinib. Daten zum Vergleich mit einer Immunchemotherapie liegen nicht vor. Eine Quantifizierung des Zusatznutzens ist auf Basis der vorliegenden Daten nicht möglich.
