Sacituzumab Govitecan beim triple-negativen Mammakarzinom
Sacituzumab Govitecan ist zugelassen zur Monotherapie des nicht resezierbarem oder metastasiertem, triple-negativem Mammakarzinom bei Patient*innen, die zuvor zwei oder mehr systemische Therapien erhalten haben, darunter mindestens eine gegen die fortgeschrittene Erkrankung. Der G-BA hat keine Subgruppen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutisches Unternehmen und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
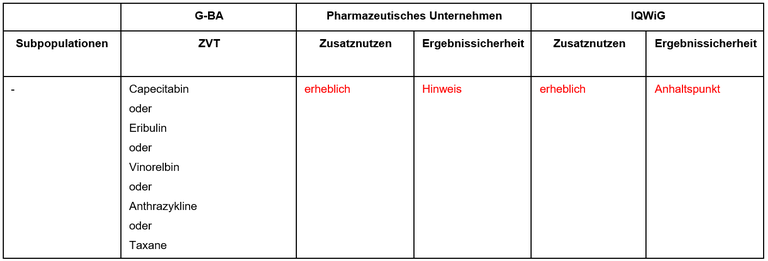
Unsere Anmerkungen sind:
- Die festgelegte, zweckmäßige Vergleichstherapie entspricht dem Standard bei Patient*innen, die für eine gezielte Therapie mit PARP- oder Immuncheckpoint-Inhibitoren nicht geeignet sind.
- Basis der frühen Nutzenbewertung zum Vergleich von Sacituzumab Govitecan vs Chemotherapie ist die internationale, multizentrische, offene Studie ASCENT. Basis des Dossiers ist der Datenschnitt vom März 2020. Aktuellere Daten liegen nicht vor.
- Sacituzumab Govitecan führte zu einer signifikanten Steigerung der Remissionsrate, zur Verlängerung des progressionsfreien Überlebens sowie der Gesamtüberlebenszeit.
- Die Nebenwirkungen entsprechen der Toxizität von Irinotecan, dem zytotoxischen Anteil dieses Antikörper-Drug-Konjugats. Im Vordergrund stehen Neutropenie und Diarrhoe.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Sacituzumab Govitecan den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
- Der IQWiG-Bericht wurde ohne Beteiligung von Fachexpert*innen und von Patient*innen erstellt. Auf Basis der eigenen Methodik wird die Festlegung eines „erheblichen“ Zusatznutzens vorgeschlagen. Die Kategorisierung ist höher als die klinische Bewertung in der ESMO Magnitude of Clinical Benefit Scale.
Die Daten etablieren Sacituzumab Govitecan als neuen Standard bei Patient*innen mit zytostatisch vorbehandeltem, metastasiertem, triple-negativem Mammakarzinom. Sacituzumab Govitecan ist auch eine Alternative zu anderen, gezielten Therapieoptionen.
