Durvalumab / Tremelimumab / Chemotherapie beim nichtkleinzelligen Lungenkarzinom
Durvalumb / Tremelimumab ist zugelassen in Kombination mit einer platinbasierten Chemotherapie bei Patientinnen und Patienten (Pat.) mit metastasiertem NSCLC ohne sensibilisierende EGFR-Mutationen oder ALK-positive Mutationen. Der G-BA hat zwei Subgruppen zur Festlegung der zweckmäßigen Vergleichstherapie gebildet und das IQWiG mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu identischen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
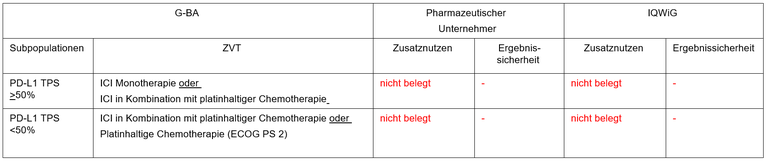
pU – pharmazeutischer Unternehmer; ZVT – zweckmäßige Vergleichstherapie; ICI – Immuncheckpoint-Inhibitor
Unsere Anmerkungen sind:
- Die Festlegung der ZVT entspricht weitgehend den aktuellen Empfehlungen der Fachgesellschaften. Allerdings kann auch bei Pat. mit anderen aktivierenden Mutationen die Indikation zu einer molekular-gezielten Erstlinientherapie bestehen, insbesondere bei reduziertem Allgemeinzustand.
- Basis der frühen Nutzenbewertung ist POSEIDON, eine multizentrische, randomisierte, offene Phase-III-Studie mit drei Armen: Durvalumab / Tremelimumab / Chemotherapie vs Durvalumab / Chemotherapie vs Chemotherapie.
- Durvalumab / Tremelimumab / Chemotherapie führte gegenüber Chemotherapie zur Steigerung der Remissionsrate sowie zur statistisch signifikanten Verlängerung der progressionsfreien und der Gesamtüberlebenszeit.
- In adjustierten, indirekten Vergleichen zeigten sich keine Unterschiede in der Gesamtüberlebenszeit gegenüber Pembrolizumab Monotherapie bei Pat. mit hoher PD-L1-Expression bzw. gegenüber Nivolumab / Ipilimumab / Chemotherapie bei Pat. mit niedriger PD-L1-Expression.
- Die Rate schwerer unerwünschter Ereignisse wurde auf 51,8 vs 44,4% im Kontrollarm gesteigert. Die Abbruchrate aufgrund von unerwünschten Ereignissen lag bei 15,5% vs 9,9% in der Kontrolle.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Durvalumab / Tremelimumab den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
Mit der Kombination Durvalumab / Tremelimumab / Chemotherapie steht eine weitere Option zur Erstlinientherapie des lokal fortgeschrittenen oder metastasierten NSCLC zur Verfügung. Belastbare, evidenzbasierte Therapieempfehlungen sind nach Vorliegen von Ergebnissen direkt vergleichender Studien möglich.
