Trifluridin / Tipiracil beim metastasierten kolorektalen Karzinom
Trifluridin / Tipiracil ist zugelassen zur Monotherapie von Patienten mit metastasiertem kolorektalem Karzinom, die bereits mit verfügbaren Therapien behandelt wurden oder die für diese nicht geeignet sind. Diese Therapien beinhalten Fluoropyrimidin-, Oxaliplatin- und Irinotecan-basierte Chemotherapien, Anti-VEGF- und Anti-EGFR-Substanzen bei geeigneter Molekularpathologie. Im ersten Verfahren war der Anhaltspunkt für einen geringen Zusatznutzen festgelegt worden. Der G-BA hat das IQWiG mit dem Bericht beauftragt. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
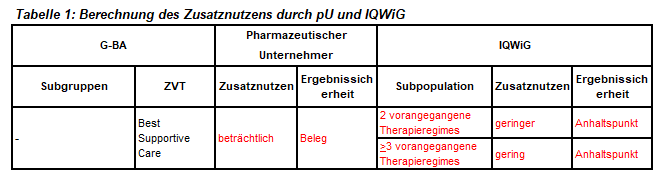
Anmerkungen sind:
- Die Festlegung der ZVT entspricht nur noch teilweise dem aktuellen Stand des Wissens und der Versorgung in Deutschland. Angemessen ist heute eine Therapie nach Maßgabe des behandelnden Arztes auf der Basis von Best Supportive Care sowie weitere systemische Therapie unter Berücksichtigung der Vortherapie und der molekularen Charakteristika des Tumors.
- Grundlage der Nutzenbewertung ist RECOURSE, eine multizentrische, internationale, randomisierte, Placebo-kontrollierte Studie mit einer 2:1 Randomisierung. Zusätzliche Studien sind TERRA, eine weitere multizentrische, internationale, randomisierte, Placebo-kontrollierte Studie mit einer 2:1 Randomisierung und TALLISUR, eine vergleichende Versorgungsstudie aus Deutschland. Die im vorherigen Dossier aufgeführte Studie J003 wird vom pU nicht in das aktuelle Dossier aufgenommen.
- Die Daten von RECOURSE haben kein publiziertes Update erfahren. Trifluridin/Tipiracil führt in RECOURSE zu einer Verlängerung der Gesamtüberlebenszeit (Hazard Ratio 0,68; Median 1,8 Monate) und der progressionsfreien Überlebenszeit (Hazard Ratio 0,48; mediane Differenz 0,3 Monate). Die Daten der weiteren Studien bestätigen diese Ergebnisse.
- Die Zeit bis zur Verschlechterung des Allgemeinzustandes mit ECOG >2 wurde durch Trifluridin/Tipiracil signifikant verlängert. Eine umfassende Analyse der Lebensqualität (Patient-reported Outcome) fehlt im Dossier.
- Schwere Nebenwirkungen im CTCAE-Grad 3/4 betreffen vor allem Laborparameter.
- Im vorherigen Bericht des IQWiG wurde eine Subgruppenbildung auf der Basis des KRAS-Mutationsstatus vorgeschlagen. Diese wird nicht wieder aufgenommen. Auf der Basis der weitgehend identischen Daten wird jetzt eine Subgruppenbildung nach der Zahl der Vortherapien vorgeschlagen. Klinisch ist dies Unterteilung sinnvoll, die Studie war aber für diese Analyse nicht gepowert.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 (Skala 1 (niedrig) – 5 (hoch)) erhält Trifluridin/Tipiracil den Grad 2.
Modul 4 im Dossier des pharmazeutischen Unternehmers hat 8.702 Seiten. Das sprengt den Rahmen.
Trifluridin/Tipiracil ist eine chemotherapeutische Option für Patienten mit vorbehandeltem, metastasiertem, kolorektalem Karzinom. Als weiteres Element der Sequenztherapie trägt es zur Verlängerung der Überlebenszeit bei.
