Frühe Nutzenbewertung von Abirateron und von Niraparib
Abirateron beim metastasierten, hormonsensitiven Prostatakarzinom
Die frühe Nutzenbewertung von Abirateron bei Patienten mit metastasiertem, hormonsensitivem Prostatakarzinom ist das dritte Verfahren zu Abirateron, aber das erste Verfahren in dieser Therapiesituation. Der G-BA hat keine Subpopulationen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu etwas unterschiedlichen, in der Gesamtbeurteilung aber ähnlichen Vorschlägen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle1:
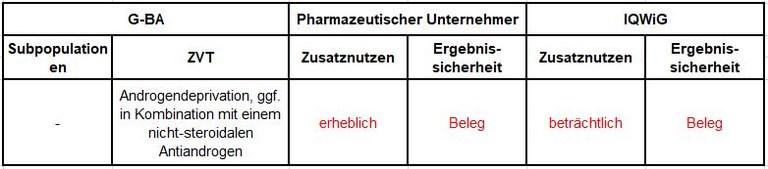
Unsere Anmerkungen sind:
- Standard beim hormonsensitiven, metastasierten Prostatakarzinom war über viele Jahrzehnte die Androgendeprivation. Das hat sich in den letzten 3 Jahren grundlegend geändert. Für eine Kombinationstherapie stehen jetzt Docetaxel und Abirateron zur Verfügung.
- Docetaxel wurde im März 2018 vom G-BA auf Vorschlag der Off-Label-Kommission auf die Liste der Arzneimittel zur Anwendung in dieser Indikation aufgenommen. Damit ist es neben der Androgendeprivation auch eine zweckmäßige Vergleichstherapie für die Nutzenbewertung von Abirateron.
- Für die frühe Nutzenbewertung von Abirateron liegen Daten von zwei großen, randomisierten Studien vor, der Zulassungsstudie LATITUDE und der Investigator-initiierten Studie STAMPEDE.
- Abirateron + Androgendeprivation führt gegenüber Androgendeprivation zu einer signifikanten, in den beiden Studien identischen Verlängerung der Gesamtüberlebenszeit mit einem Hazard Ratio von 0,62 in der Metaanalyse. Leider fehlen Daten zur Postprogressionstherapie. Zugelassene Arzneimittel wie Docetaxel, Enzalutamid, 223Radium und Cabazitaxel können in späteren Krankheitsstadien ebenfalls die Überlebenszeit verlängern.
- Abirateron führt auch zur Verlängerung des progressionsfreien Überlebens und zur Verbesserung von Parametern des Patient-Reported-Outcome.
- Die Rate schwerer Nebenwirkungen ist unter Abirateron höher als unter Androgendeprivation. Klinisch relevant sind Hypertonie und Hypokaliämie.
Abirateron führt in Kombination mit Androgendeprivation zu einer Verbesserung der Prognose von Patienten mit metastasiertem, hormonsensivem Prostatakarzinom. Die Verlängerung der Überlebenszeit ist der von Docetaxel vergleichbar. Unklar ist zurzeit, welche Patienten eher von Abirateron und welche Patienten eher von Docetaxel profitieren.
Niraparib in der Erhaltungstherapie des Platin-sensitiven Ovarialkarzinoms
Das Verfahren zu Niraparib (Zejula®) bei Patientinnen mit fortgeschrittenem Ovarialkarzinom ist das zweite Verfahren in dieser Entität. Niraparib gehört zur Substanzklasse der Poly(ADP-ribose) Polymerase (PARP)–Inhibitoren. Niraparib ist zugelassen für die Erhaltungstherapie bei rezidivierten Patientinnen mit gering differenziertem, serösem Karzinoms der Ovarien, der Tuben oder mit primärer Peritonealkarzinose, die erneut auf eine Platin-haltige Chemotherapie angesprochen haben, d. h. eine komplette oder partielle Remission erreicht haben. Niraparib hat einen Orphan-Drug-Status, eine Vergleichstherapie wurde vom G-BA nicht festgelegt. Der pharmazeutische Unternehmer beantragt einen beträchtlichen Zusatznutzen. Der G-BA Bericht enthält keinen Vorschlag zur Kategorisierung des Zusatznutzens. Er listet in seiner Zusammenstellung keine Effekte bei der Morbidität, keine positiven oder negativen Effekte bei der Mortalität, und negative Effekte bei den Nebenwirkungen auf. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle1:
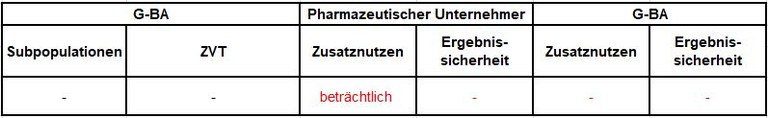
Unsere Anmerkungen sind:
- Basis der frühen Nutzenbewertung ist NOVA, eine internationale, randomisierte, Placebo-kontrollierte Studie mit einer 2:1 Randomisierung zugunsten des Niraparib-Arms.
- Niraparib führt sowohl bei Patientinnen mit als auch ohne BRCA1/2-Mutationen zu einer deutlichen Verlängerung des progressionsfreien Überlebens mit einem Hazard Ratio von 0,27 bzw. 0,38. Dies führt auch zur Verlängerung der Zeit bis zur nächsten Therapie.
- Niraparib führt nicht zur Verlängerung der Gesamtüberlebenszeit.
- Die Rate schwerer Nebenwirkungen liegt bei 74,1%, die Rate von Therapieabbrüchen aufgrund von Nebenwirkungen bei 14,7%. Die Mehrzahl schwerer Nebenwirkungen von Niraparib ist hämatologisch, ohne klinische Symptomatik.
Mit Niraparib und Olparib sind jetzt zwei wirksame PARP-Inhibitoren zur Erhaltungstherapie bei Patientinnen mit rezidiviertem, serösem Ovarialkarzinom, die erneut auf eine Platin-haltige Chemotherapie angesprochen haben, zugelassen. Die Wirksamkeit erscheint vergleichbar, Daten aus direkt vergleichenden Studien liegen bisher nicht vor. Niraparib hat die breitere Zulassung, ist aber auch mit mehr Nebenwirkungen belastet. Die Nebenwirkungen sind vor allem laborchemisch, nicht klinisch manifest.
